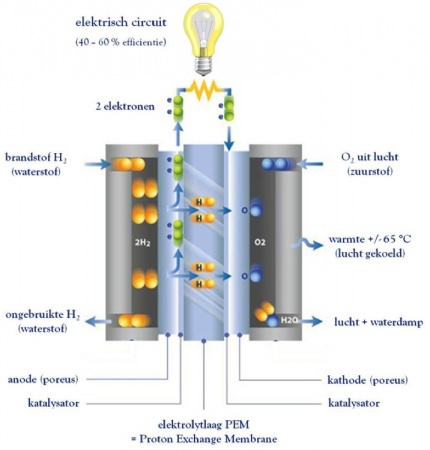
Hoe werkt een brandstofcel
In het opzicht van chemische energie omzetten naar elektrische energie lijkt een brandstofcel op een batterij. Toch is er een belangrijk verschil tussen een batterij en een brandstofcel. In een brandstofcel kunnen namelijk steeds opnieuw reagentia (bijvoorbeeld: waterstof en zuurstof) van buitenaf worden aangevoerd, terwijl de reagentia in een batterij opgeslagen zitten in een gesloten stelsel. Een brandstofcel blijft dus werken zolang zij aangesloten is. Een batterij werkt niet meer als de reagentia opgebruikt zijn. Daarbij is een batterij op zich alleen al een grote belasting voor het milieu.
Een brandstofcel bestaat uit 2 elektrodes. Een poreuze positieve anode (= pool of elektrode waar de elektronen uitkomen) en een poreuze negatieve kathode (= pool of elektrode waar de elektronen ingaan). In de cel worden deze twee elektrodes door een membraan (elektrolytlaag) gescheiden. Waterstof en zuurstof worden afzonderlijk van elkaar aan de brandstofcel toegevoerd. In het geval van een brandstofcel met een zure elektrolytlaag vinden de volgende elementaire elektrochemische reacties plaats. Met behulp van een katalysator vindt aan de anode de oxidatie van waterstof plaats, wat betekent dat waterstofmoleculen (H2) gesplitst worden in 2 waterstofionen (2 H+) en twee elektronen (2 e-). De elektronen stromen vervolgens via een elektrisch circuit naar de kathode: dit is de elektrische stroom die gebruikt kan worden om bijvoorbeeld een lamp te doen branden. De H+-ionen (protonen) bewegen zich door de elektrolytlaag naar de kathode. Ondertussen worden aan de kathode van de brandstofcel zuurstofmoleculen (O2) gereduceerd tot zuurstofionen (O2-). Bij de opname van de elektronen, die afkomstig zijn van de anode, en de aangevoerde H+-ionen via de elektrolytlaag wordt, in een zure brandstofcel aan de kathode water en warmte gevormd. In de meeste brandstofcellen kan aan de kathode lucht toegevoerd worden in plaats van zuivere zuurstof. Uit de lucht wordt namelijk enkel de zuurstof verbruikt.
Hierbij een overzicht van de chemische reacties die in een brandstofcel plaatsvinden:
anode kathode
2H2 → 4H+ + 4e- O2 + 4H+ + 4e- → 2H2O
gehele cel
2H2 + O2 → 2H2O + energie (= elektriciteit en warmte)
Rendement
In brandstofcellen zijn hogere rendementen mogelijk dan in gewone verbrandingsmotoren of stoommachines doordat de energieomzetting niet verloopt volgens de Carnotcyclus. In de Carnotcyclus wordt de chemische energie namelijk eerst in warmte omgezet en pas daarna in bijvoorbeeld elektrische energie.
Vergelijking tussen de 2 processen:
Brandstofcel: Chemische energie → Elektrische energie
Carnotcyclus: Chemische energie → Warmte → Elektrische energie
Bij de laatste stap treden noodzakelijkerwijs grote verliezen op, doordat altijd maar een deel van de warmte in arbeid kan worden omgezet.
Bij brandstofcellen is dit niet het geval. Toch treden er ook in brandstofcellen omzettingsverliezen op omwille van een aantal ongewenste nevenreacties.
Eén enkele brandstofcel levert in theorie een spanning van ongeveer 1,23 volt, maar in de praktijk ligt die spanning veel lager; tussen de 0,5 en 0,9 volt. Hierdoor zal één brandstofcel van 1,23 volt een maximum rendement hebben van 75%. Wat betekent dat deze maximum 0,92 volt zal leveren.
Om de spanning te verhogen worden de afzonderlijke cellen op elkaar gestapeld en in serie geschakeld. De stapel die zo ontstaat wordt een "brandstofcel-stack" of kortweg "stack" genoemd. Hierdoor zal een stack van bijvoorbeeld 50 cellen in serie, (400 cm2 werkzaam oppervlak/cel), een elektrisch vermogen hebben van 4800 W.